MnO2+4HCl(浓)=====MnCl2+Cl2(上升)+2H2O 氧化剂和还原剂的物质量之比是多少
来源:学生作业帮 编辑:搜搜做题作业网作业帮 分类:化学作业 时间:2024/05/16 01:14:19
MnO2+4HCl(浓)=====MnCl2+Cl2(上升)+2H2O 氧化剂和还原剂的物质量之比是多少
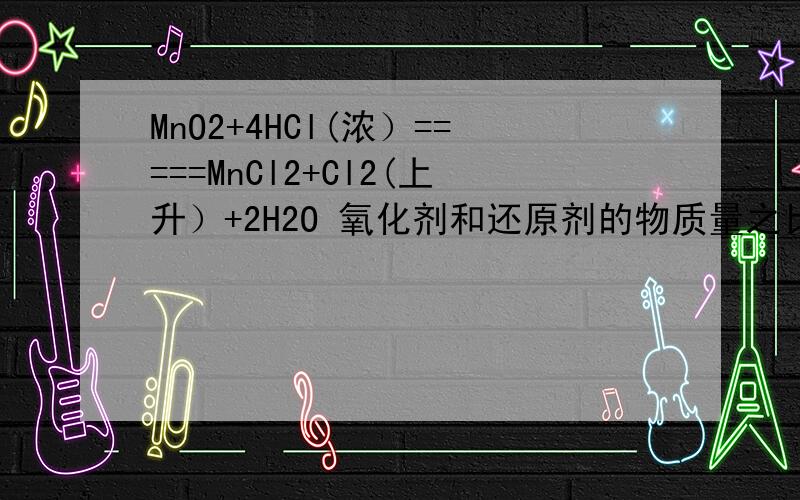
氧化剂为MnO2 还原剂为HCl
氧化剂和还原剂之比为1:2 因为只有两个氯离子被氧化 一个锰被还原
氧化剂和还原剂之比为1:2 因为只有两个氯离子被氧化 一个锰被还原
MnO2+4HCl(浓)=====MnCl2+Cl2(上升)+2H2O 氧化剂和还原剂的物质量之比是多少
4HCL(浓)+MnO2===MnCL2+CL2↑+2H2O 氧化剂还原剂物质量比
下列反应是实验室制取Cl2的反应:MnO2+4HCl(浓)==MnO2+Cl2+2H2O 氧化剂和还原剂物质的量之比是(
mn02+4hcl(浓)=mncl2+cl2↑+2h2o,当制取1molcl2时,所需氧化剂与还原剂物质的量之比
在MnO2+4HCl==MnCl2+Cl+2H2O中,氧化剂与还原剂物质的量之比为( )
MnO2+4HCl(浓)===MnCl2+2H2O+Cl2↑ 氧化剂与还原剂是什么
MnO2+4HCl---MnCl2+Cl2+2H20 氧化剂与还原剂物质的量之比
MnO2+4HCl(浓)=MnCl2+Cl2(上箭)+2H2O求氧化剂和还原剂的质量之比,氧化产物和还原产物的物质的量之
MnO2 + 4 HCl (浓) == MnCl2 + Cl2 + 2 H2O 中氧化剂 ,还原剂 ,氧化产物 ,转移电
MnO2+4HCl(浓)=(条件:加热)MnCl2+Cl2+2H2O.氧化剂,还原剂,氧化产物,还原产物分别是什么?
4HCl+MnO2 =Cl2+MnCl2+2H2O中MnO2的物质的量为什么和Cl2的物质的量相等
4HCl(浓)+MnO2=MnCl2+Cl2+2H2O