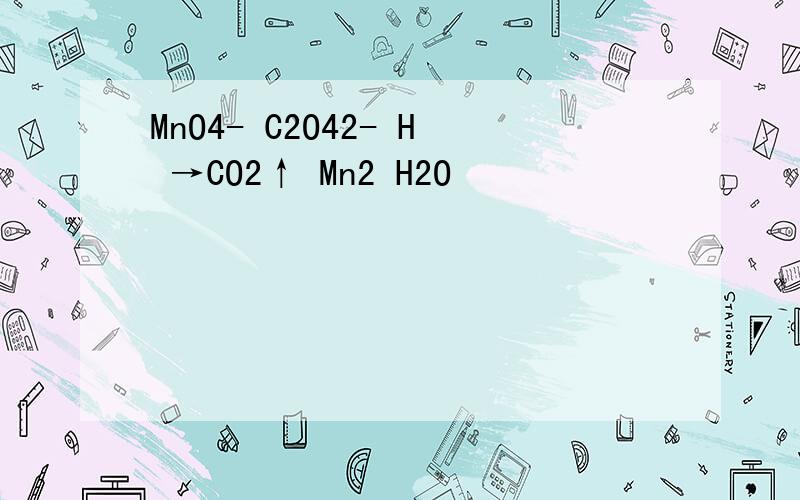
MnO4- C2O42- H →CO2↑ Mn2 H2O
来源:学生作业帮助网 编辑:作业帮 时间:2024/04/29 04:25:59
你题目打错了吧,溶液呈弱酸性,氢氧根浓度一定小于氢离子浓度再问:看这道题,第30大题第二问第二步就是氢氧根浓度大于氢离子浓度,http://wenku.baidu.com/view/86a55cdd6
草酸是有机酸的二羧基酸类,也是有机酸中强酸之一.与浓硫酸作用则失去水分,分解为二氧化碳和一氧化碳.草酸还有还原性,与氧化剂作用易被氧化成二氧化碳及水,与碱类起中和作用,生成草酸盐.在强酸的环境下,3价
楼主多想了,其实这个配平就是高锰酸根在酸性作用下把双氧水氧化.因为它的氧化性极强的.此时的双氧水只作为还原剂,所以:化学式右面的氧气全部来自双氧水(不然的话,不需要双氧水,只要酸性就可以使高锰酸根自身
剩下就是原子个数守恒呀.2个MnO4-有8个O所以有8个H2O;需要16个H,5个H2O2已经有10个H,所以H+的系数就是6.【2MnO4-】+【5H2O2】+【6H+】=【2Mn2+】+【5O2】
随便写一个:5FeCl2+KMnO4+8HCl==5FeCl3+MnCl2+4H2O
这里Mn(2+)转移电子给S2O8(2-)所以Mn(2+)是还原剂,S2O8(2-)是氧化剂根据电子守恒定律,Mn(2+)转换为MnO4(-)移动5个电子S2O8(2-)转换为SO4(2-)移动2个电
Mn为+7价,变为+2价,降5.O-1价,变为0价,2个O升高2.电子数Mn*2=O*5,再根据H个数配平水,2(MnO4-)+5H2O2+6(H+)====2(Mn2+)+5O2+8H2O
MnO4-中的O不是变为O2中的0价,O2来自H2O22MnO4-+5H2O2+6(H+)→2(Mn2+)+5O2+8H2O
不能共存H与AlO2会生成Al(OH)3
5个O2中的氧都是来源于H2O2中的O,因为是H2O2中-1的O被氧化后形成了O2所以H2O2系数为5,这样根据O守恒H2O系数为8,根据H守恒H+离子系数为62MnO4-+5H2O2+6H+----
MnO4-+8H++5e-=Mn2++4H2O*2H2O2-2e-=2H++O2*52MnO4-++5H2O2+6H+=2Mn2++5O2+8H2O上面是正确答案
总反应:2MnO4-(aq)+5H2O2(aq)+6H+(aq)→2Mn2+(aq)+5O2(g)+8H2O(l)MnO4-(aq)+8H+(aq)+5e=Mn2+(aq)+4H2O(l)还原反应5H
(2)溶液颜色由无色(原溶液的颜色)变成紫红色(高锰酸钾的颜色),由第一问可以算出25mL溶液中n(C2O42-)(3)由质量守恒n(H2C2O4·2H2O)+n(KHC2O4)=10n(C2O42-
2【MnO4-】+10【I-】+16【H+】=2【Mn2+】+5【I2】+8【H2O】
2MnO4-+5H2O2+6H+==8H2O+5O2+2Mn2+
H+、Cu2+、H2O;能接受电子F-、OH-、C2O42-、BF3、SO3、H2O.能给出电子
配平相信你没问题了,就解决下面的计算吧.1.消耗了0.25mol/LNaOH20mL,物质的量是0.005mol,所以中和的H+就是0.005mol了2.颜色应该是由紫红色变为无色,经过计算酸性高锰酸
似乎你的MnO4应该为(MnO4-)(一)下面的是按照MnO4得到的结果MnO4+H2O2+(H+)→(Mn2+)+O2+H2O如何配平先假设(Mn2+)前面的系数是2(其实只要是正数就可以了).得到
第一种,Al3+NO3-MnO4-Fe3+NH4+H+第二种,Na+K+OH-S2-CO32-SO32-